Книги по аквариумистике
Лучшая on-line библиотека для начинающих и профессионалов!
Круговорот азота
Важным питательным соединением солью являются нитраты, поглощаемые растениями из воды. Таким образом азот участвует в круговороте веществ. Азот, поступающий с кормом, всегда находится в составе сложных химических структур, – в молекулах белков, пептидах, аминокислотах, в хлорофилле, в рибонуклеиновых кислотах (РНК), дезоксирибонуклеиновых кислотах (ДНК) и отчасти также в витаминах. Азот необходим в различных ключевых аспектах жизни, например, фотосинтез, образование белка, воспроизведение рода. Например, образование хлорофилла прекращается при отсутствии доступного азота. Планктон с большим трудом получает необходимое количество азота, концентрируя азот, содержащийся в воде, в 30 – 50 тысяч раз, в то время как углерод концентрирует в 2000 раз. С экскрементами или погибшими животными в воду поступают готовые органические соединения, прежде всего белок. Bacterium coli, Bacterium proteus, Bacterium subtilis переводят белки в пептиды и аминокислоты. Ученые различают два разных вида аминокислот. Группа аминокислот, содержащих серу, обладает сильными восстанавливающими свойствами и может при больших количествах значительно снижать окислительно-восстановительный потенциал. При анаэробных условиях в этом случае может образовываться сероводород (H2S), чему способствует очень толстый слой мелкозернистого грунта на дне аквариума. Ароматические аминокислоты имеют слабые восстановительные свойства, но легко окисляются. В качестве промежуточных продуктов образуются фенолы и крезолы, из которых первые весьма ядовиты. Фенолы, однако, легко окисляются до неопасных меланинсодержащих красителей.
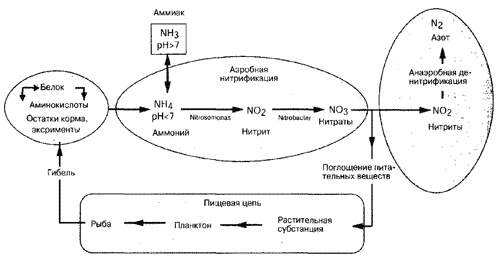
Цикл азота охватывает трофическое разложение органических веществ и процессы нитрификациии и денитрификации
Бактерии переводят аминокислоты в амины, которые бактериями опять превращаются в органические кислоты и аммиак. Если накапливаются органические кислоты в высоких концентрациях, то может временно понизиться значение pH до такой степени, что бактерии относительно быстро трансформируют органические кислоты в угольную кислоту и воду. На следующем этапе в круговороте участвует аммоний или, в зависимости от значения pH, аммиак. В частности, у морских животных выделения сильно сконцентрированы и содержат до 80 мг азота на 100 мл. Основным компонентом в выделениях, от 20% до 50%, является аммоний. Аммоний (NH4+) может существовать и как аммиак, но следует знать, что в этой форме он высоко токсичен. Будет ли присутствовать аммоний, или аммиак, или обе формы в воде аквариума, как правило, зависит от значения pH. Рисунок вверху показывает, что соотношение между двумя формами смещает значение pH. В области значений pH, которая пригодна для аквариума (в морской воде примерно pH 9), токсичный аммиак содержится в небольших количествах, примерно 20%. Конечно, следует учитывать, что аммиак действует уже в малых концентрациях. Лососи особенно чувствительны к нему и реагируют уже при содержании 0,006 мг на литр. Чем ниже значение pH, тем меньше содержания аммония. Уже при pH 7 его содержится только примерно 0,5%. Повышенная температура может увеличить содержание аммиака. Таким образом, понятно, почему в аквариумах с теплой морской водой таится опасность. При температуре 250 °C и при значении pH 8,4 содержится уже 10% аммиака. По этой же причине опасны жесткие пресные воды, которые могут показывать аналогичные концентрации аммиака. Особенно нужно обратить внимание на то, что кривые на диаграмме изображены в логарифмическом масштабе. В то время как смещение значения pH с 6 до 6,3 не влияет на концентрацию аммиака, смещение pH с 8 до 8,3 повышает его содержание с 5% до 10%. То есть оно удваивается! Смещение значений pH такого же порядка в аквариумах, густо населенных растениями, из-за ассимиляции может происходить в течение дня без последствий. Подобное происходит в аквариумах, которые заняты преимущественно беспозвоночными. Трансформация аммония/аммиака посредством бактериального окисления приводит к образованию нитритов. Этот процесс осуществляют аэробные бактерии Nitrosomonas. Для того чтобы существовать и окислять аммоний и аммиак в нитриты, им необходима вода, богатая кислородом:
Nitrosomonas
NH4+ + 1,5O2 => NO2– + 2H+ + H2O + Энергия
Это уравнение показывает потребность в кислороде. Это уникальное окисление возможно только с помощью бактерий.
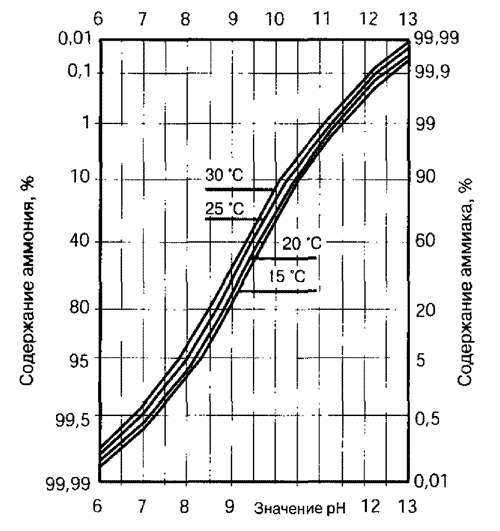
Соотношение аммония и аммиака в воде зависит от pH и температуры
Растворенный в воде кислород самостоятельно не может окислять аммоний и аммиак. Гораздо более активный озон только при высоких значениях pH в состоянии это делать. Но из этого уравнения также ясно, что бактерии окисляют аммиак не без пользы для себя. Они живут за счет освобождающейся энергии. Подобно им действуют аэробные бактерии Nitrobacter, которые нитриты перерабатывают далее в нитраты. Такое простое условие, как «вода, богатая кислородом», к сожалению, часто не учитывается при конструировании фильтров всех видов. Даже если приведенные уравнения реакций для дилетанта не очень наглядны, для понимания процесса в биологическом фильтре они очень важны.
NO2– + 0,5O2 => NO3–
Вместе с тем можно представить некоторые расчеты. Ионная масса аммония NH4+ равна 18. Чтобы окислить эту массу бактериям нужно 1,5 молекулы кислорода с общей массой 48. Итак, чтобы один миллиграмм аммония окислить до нитритов необходимо 2,6 мг кислорода! Если провести подобные расчеты для окисления нитритов в нитраты, то можно установить, что требуется только 0,35 мг кислорода для 1 мг нитритов. Для проведения этой реакции необходима гораздо меньшая потребность в кислороде, и на практике она протекает значительно легче. Связь между потребностью в кислороде и скоростью нитрификации изображена на верхнем рисунке. Если нитрификаторы получают кислорода меньше, чем им это необходимо, они ограничивают свою деятельность. Итак, установлено, что обе реакции притекают только в среде, обогащенной кислородом! Если мы еще раз посмотрим на верхнее уравнение, то увидим, что одним из продуктов реакции являются свободные ионы водорода! Не бойтесь, наш биологический фильтр не взорвется, но, как указывалось ранее, повышение концентрации ионов водорода снижает значение pH. Ион водорода не остается в свободном состоянии, а реагирует по следующему уравнению с бикарбонатом, в результате чего получается оксид углерода и вода:
H+ + HCO3– => CO2 + H2O
Следовательно, хорошо работающий биофильтр может лишь незначительно понижать значение pH. Это не должно нас беспокоить, так как этот эффект в морской воде и в жесткой пресной воде может легко устраняться с помощью фильтровального материала, содержащего известь.
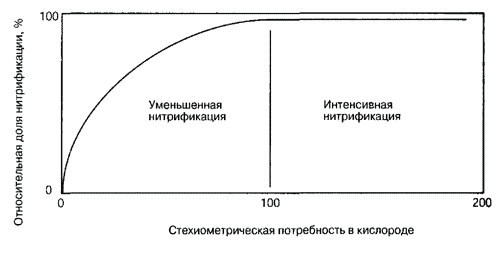
Интенсивность нитрификации зависит от имеющегося в среде кислорода
Предыдущая || Следующая || Оглавление